В настоящее время принятой стратегией коррекции сахарного диабета (СД) и инсулинорезистентности является медикаментозная терапия, направленная на доставку инсулина извне, на стимуляцию секреции собственного инсулина и снижение концентрации глюкозы крови. Однако, многие препараты способствуют снижению уровня глюкозы крови, увеличению секреции инсулина, однако обладают многочисленными побочными воздействиями. В связи с этим перспективным подходом видится использование генной терапии для коррекции СД.
Генная терапия направлена на лечение заболеваний с использованием внесения одной или нескольких терапевтических нуклеиновых кислот в клетки пациента или путем исправления дефектных генов с помощью, например, систем редактирования генома [1].
Разделяют два способа воздействия генных конструкций на клетки-мишени – in vivo (в организме) и ex vivo (вне организма). В первом случае – непосредственно на тканях живого организма с использованием адресной доставки нуклеиновых кислот и преодолением сложных проблем, связанных с быстрым разрушением чужеродного биологического материала. Во втором случае воздействие основано на генотерапевтической модификации вне организма определенных клеток с последующим их возвратом в системный кровоток или пораженный орган [2].
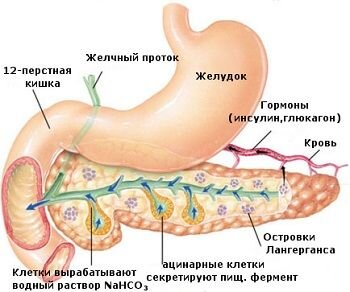
Основными мишенями генной терапии СД являются: стимуляция восстановления островков Лангерганса (участков поджелудочной железы, в которых вырабатывается инсулин) и выработка вещества лептин, который способствует снижению аппетита и массы тела и, напротив, повышению чувствительности к инсулину.
Генно-терапевтический подход обладает значительным преимуществом перед медикаментозной терапией СД – отсутствием необходимости постоянно с небольшими интервалами времени принимать препарат, что, в сочетании с высокой специфичностью и, как следствие, широкими возможностями регуляции обмена веществ, делает генно-терапевтический подход к коррекции СД перспективнейшим направлением [1].
Эффективность генной терапии СД уже доказана в экспериментах на животных. Например, было показано, что у крыс с сахарным диабетом клетки кишечника и печени, измененные с помощью генно-инженерных технологий, способны производить инсулин в достаточных количествах, чтобы поддерживать нормальный уровень сахара в крови [3].
В свою очередь, американские медики разработали генную терапию для лечения синдрома Вольфрама – одной из самых тяжелых форм диабета, и проверили ее в действии на мышах. Синдром Вольфрама – это редкая генетическая болезнь, которая связана с появлением ряда мутаций в генах WFS1 и CISD2. У носителей этих мутаций часто еще в детстве появляется диабет первого типа, в подростковом возрасте у них пропадают слух и зрение, а также возникает ряд других тяжелых проблем с работой нервной системы. Ученые с помощью новых технологий исправили в геноме "опечатку" в гене WFS1 и потом использовать их для того, чтобы выращивать так называемые бета-островки Лангерганса поджелудочной железы, которые вырабатывают инсулин. Опыты показали, что уровень сахара в крови грызунов начал нормализоваться всего через две недели после того, как ученые ввели в поджелудочную железу "заготовки" бета-островков Лангерганса. Это подтвердило эффективность подобного подхода. В следующие полгода состояние мышей продолжало оставаться стабильным. Это говорит о том, что бывшие стволовые клетки успешно прижились в их организме и стали частью поджелудочной железы. Подобный успех, как считают ученые, открывает дорогу не только для лечения синдрома Вольфрама, но и "обычного" диабета первого типа [4].
Опыта применения технологий редактирования гена у людей пока нет. Переходом к нему могут стать испытания устройства ViaCyte, предоставляющего собой контейнер со средой для развития, поддержки и обеспечения жизненных потребностей модифицированных клеток, производящих инсулин. Контейнер обладает полупроницаемыми стенками, способными пропускать инсулин, кислород и питательные вещества, но препятствующими проникновению клеток [3]. Предполагается, что устройство будет имплантироваться под кожу, в рамках простой амбулаторной операции. Затем клетки, внедренные в тело, вырастут в полноценные клетки поджелудочной железы и начнут секретировать инсулин, и регулировать уровень сахара в крови [5]. Клинические испытания по трансплантации ViaCyte как перспективного вида лечения СД 1 типа уже начались. Нам остается дождаться их результатов и внедрения этой новинки в жизнь.
https://dzen.ru/a/ZF5bDNgNQUkp1pKu